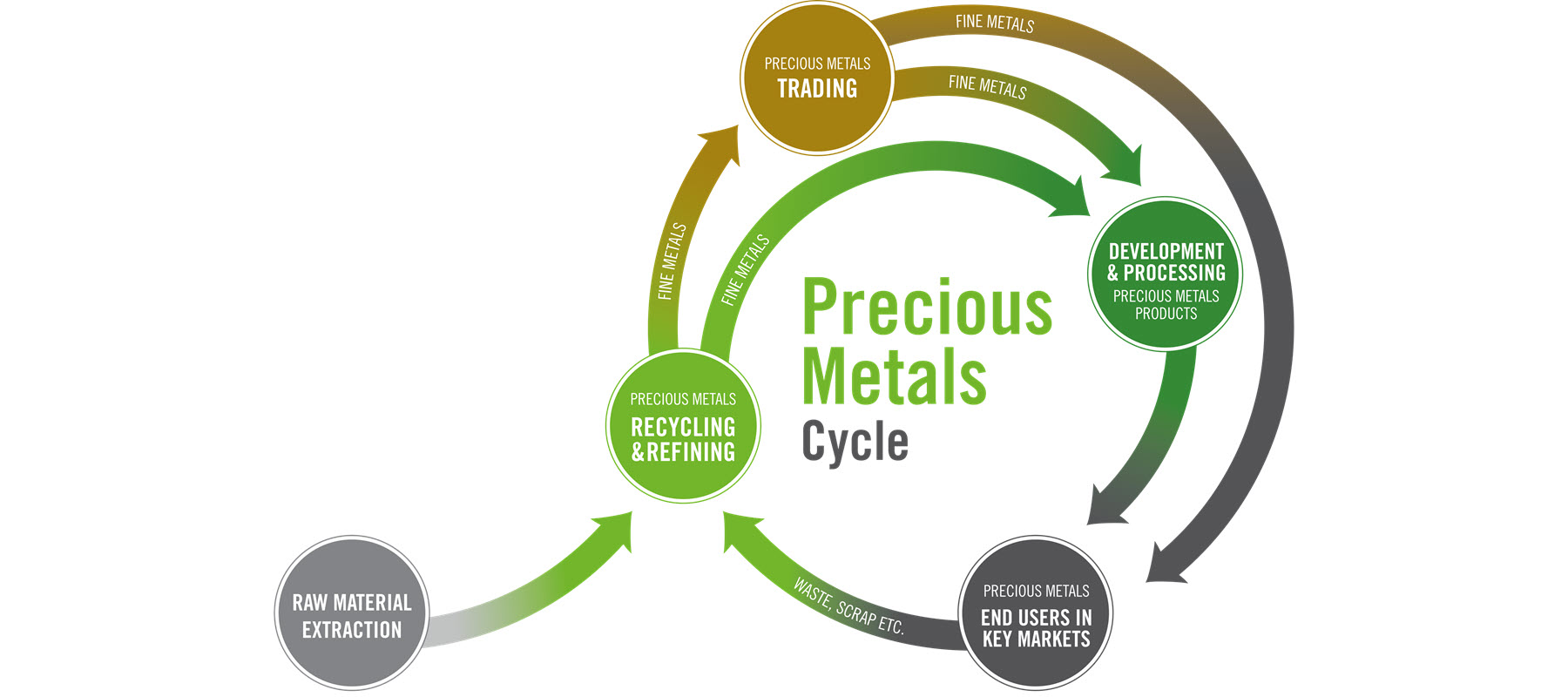
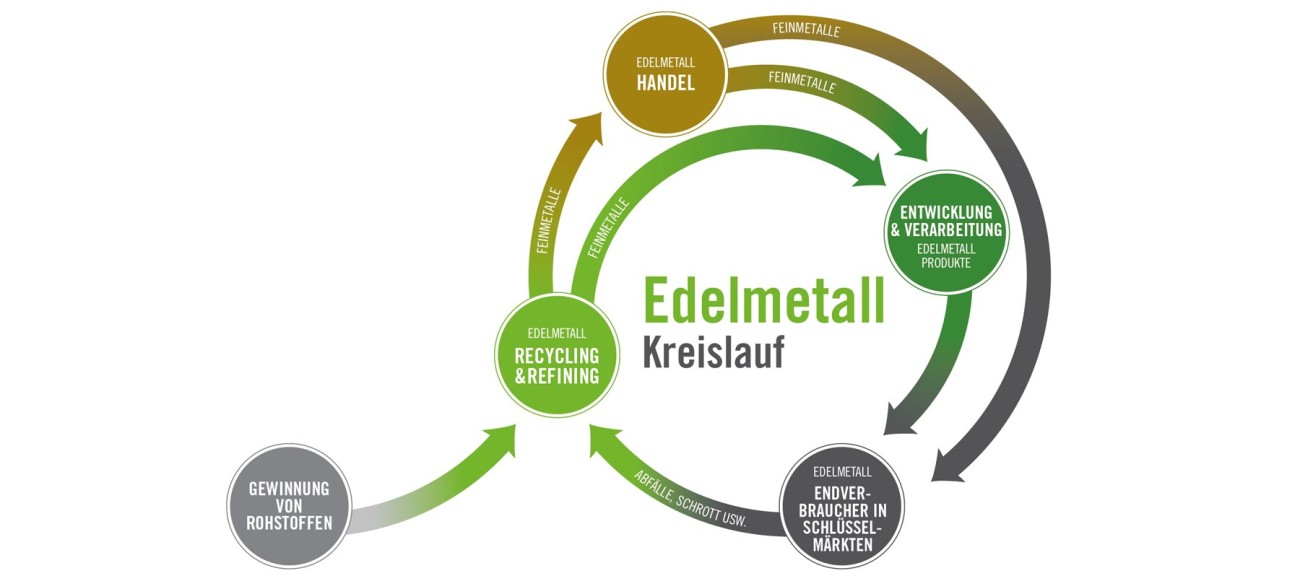
Heraeus Precious Metals ist einer der weltgrößten Refiner von Edelmetallen und gehört zu den führenden Adressen im industriellen Edelmetallhandel. Unsere Edelmetallprodukte finden in vielfältigen Industrien Verwendung, darunter Automobil-, Chemie-, Halbleiter-, Pharma-, Wasserstoff- und Schmuckindustrie. Aufgrund unserer langjährigen Erfahrung und technischen Expertise bieten wir Lösungen und Produkte in höchster Qualität. Dabei stehen wir unseren Kunden als zuverlässiger Entwicklungspartner zur Seite und finden die beste Lösung für seine Anforderungen.
Mit fünf Handels- und 14 Produktions- und Recyclingstandorten in allen wichtigen Zeitzonen bieten wir unseren Kunden ein globales Produktions- und Logistiknetzwerk. Vertrauen und Zuverlässigkeit, die strikte Einhaltung führender Compliance-Standards, Transparenz und unsere finanzielle Stabilität bilden seit mehr als 170 Jahren die Grundlage unseres Geschäfts.